Kenapa kita harus mengambil vitamin C iaitu asid askorbik, untuk melindungi daripada virus berjangkit seperti wabak baru manusia koronavirus di Wuhan, China [1]?
Jawapannya terletak pada cara bagaimana C***navirus mempengaruhi fungsi mitokondria, dan bagaimana vitamin C, asid askorbik (AA) melindungi dan meningkatkan rangkaian pertahanan yang komprehensif daripada sokongan imun kepada integriti bioenergetik mitokondria.
Peranan Asid Ascorbic Dalam Pertahanan Badan
Asid askorbat (AA) telah lama dikenali sebagai antioksidan, dengan keupayaan meningkatkan imuniti [2].
Pemahaman yang lebih baru menunjukkan bagaimana melindungi AA daripada serangan oleh patogen dengan memperkuat pertahanan epitel, sementara menyokong kedua-dua sistem imun yang bersifat bawaan dan adaptif, mempertahankan tubuh terhadap mikrob yang menyerang [4].
Leucocytes termasuk neutrofil telah ditunjukkan untuk mengumpul sejumlah besar AA. Meningkatkan suplemen asid askorbik, menyebabkan peningkatan motilitas neutrofil pada pesakit dengan jangkitan berulang [5]. Pengumpulan asid askorbik dalam neutrofil menyebabkan kemoterapi, fagositosis, dan membunuh mikroba yang lebih baik, manakala penurunan nekrosis / NETOSOS dan kerosakan tisu yang berpotensi [4].
Badan yang semakin meningkat bukti menunjukkan kemungkinan bahawa AA secara positif boleh mempengaruhi perkembangan dan fungsi limfosit dengan merangsang pembezaan dan percambahan sel B dan T [6, 7,8].
Ia tidak menghairankan bahawa jangkitan boleh mengurangkan kadar asid askorbik dengan ketara [9]. Dua ujian terkawal mendapati tindak balas yang bergantung kepada dos penting dalam perencatan simptom sejuk biasa apabila asid askorbik telah ditambah sehingga 8 g / hari [10].
Keupayaan asid askorbik untuk mempengaruhi sistem imun mungkin hanya sebahagian daripada cerita bagaimana ia dapat melindungi kita daripada virus berjangkit seperti C***na virus.
Untuk memahami sepenuhnya bagaimana fungsi AA, kita perlu sedar bahawa AA bukan hanya antioksidan, ia adalah molekul REDOX, yang digunakan oleh badan kita untuk mengimbangi pertukaran elektron dalam proses biokimia yang penting. Ini sebenarnya adalah kunci untuk memahami bagaimana AA berfungsi sepenuhnya di dalam badan kita.
C***navirus, Ribut Cytokin & Apoptosis – Cerita Mengenai Membran Mitochondrial
C***navirus novel 2019 (2019-nCoV), yang dikenalpasti dalam pesakit dengan radang paru-paru virus muncul pada akhir Disember 2019 di Wuhan, China [17] adalah betaC***navirus yang menanggung 88% identiti kepada dua coronavirus seperti sindrom pernafasan akut pernafasan yang teruk, bat-SL-CoVZC45 dan bat-SL-CoVZXC21, kedua-duanya dikumpulkan pada tahun 2018 di Zhoushan, timur China [11].
C***naviruses (CoVs) dibungkus, virus RNA tunggal terkandas dibahagikan kepada empat subtipe AlphaC***navirus (αCoV), BetaC***navirus (βCoV), DeltaC***navirus (δCoV), dan GammaC***navirus (γCoV) [12]. Alpha dan beta CoVs berasal dari kelawar dan tikus manakala delta dan gamma CoVs berasal dari spesies burung.
CoVs menjadi patogen penting kerana ia boleh menyebabkan sindrom pernafasan akut yang teruk (SARS), seperti wabak yang menjangkiti 8000 pesakit yang menyebabkan 800 kematian di China pada tahun 2002-2003. MERS-CoV yang bertanggungjawab untuk wabak berterusan di Semenanjung Arab sejak 2012 [13] dan SARS-CoV kedua-duanya berasal dari kelawar dan melompat ke tuan rumah lain mamalia sebelum melintasi halangan spesies untuk menjangkiti manusia.
Ketegangan novel ini dari Wuhan, China hanya mempunyai persamaan 79% kepada SARS-CoV (2002-2003) dan persamaan 50% kepada MERS-CoV (2012) [11].
Walau bagaimanapun, kedua-dua SARS-CoV [14] dan 2019-nCoV dapat mengikat kepada angiotensin penukar enzim 2 reseptor (ACE2) pada manusia [15, 16].
Kemasukan sel adalah komponen utama penghantaran silang spesies, terutamanya untuk β-CoVs [40]. Peranan reseptor ACE2 adalah penting kerana ia adalah cara yang mana betakoronavirus (βCoV) seperti SARS-CoV dan 2019-nCoV dapat masuk ke dalam sel manusia [18]. Malangnya, reseptor ACE2 bukan satu-satunya laluan masuk βCoVs ke dalam sel tuan rumah.
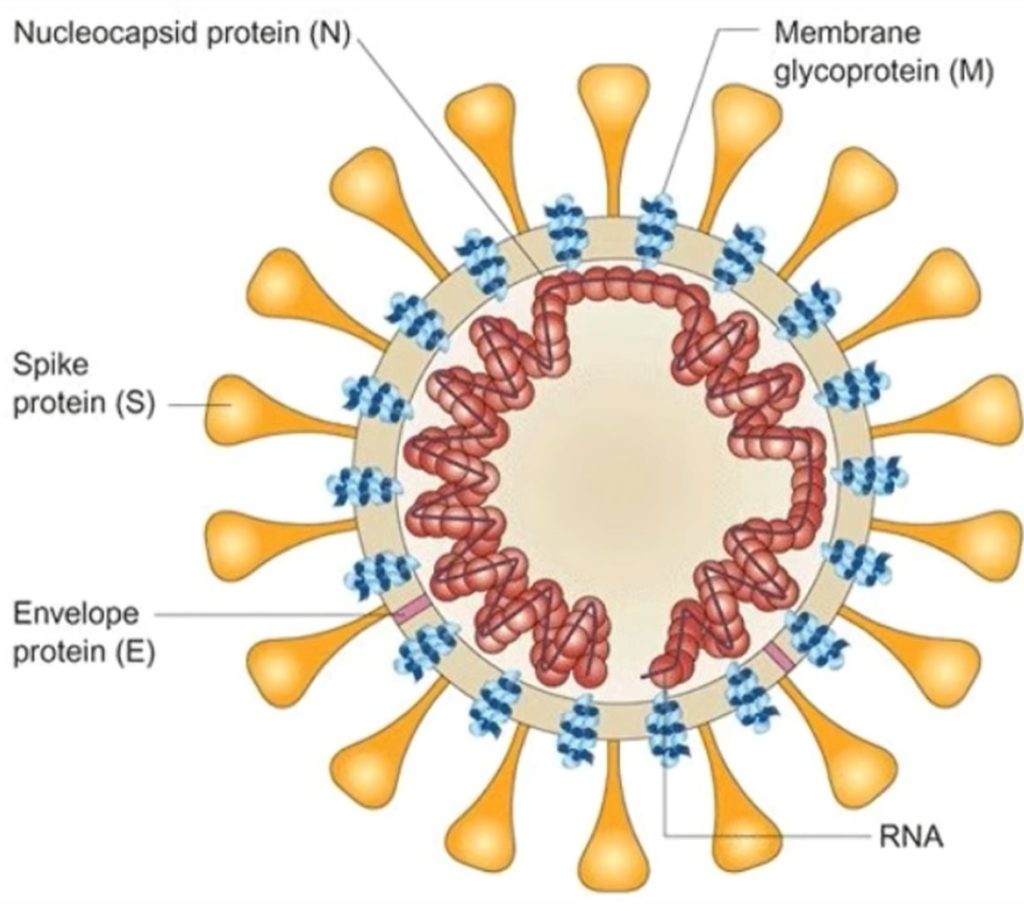
Protein Sampel dan Ketumpatan Membran
The 2019-nCoV dan C***navirus lain seperti SARS-CoV menyandikan protein yang dikenali sebagai protein sampul (E) yang boleh memodifikasi kebolehtelapan membran sel tuan rumah untuk mendapatkan masuk ke dalam sel tuan rumah, mempromosikan replikasi, pelepasan dan percambahan. Protein ini dapat membentuk saluran ion untuk mendorong perubahan kebolehtelapan membran [19, 23].
Dalam SARS-CoV, protein E telah diperhatikan untuk translocate ke permukaan sel dan sebahagiannya dikaitkan dengan rakit lipid [20]. Protein sampul (E) ini memainkan peranan yang berlainan dalam morphogenesis C***navirus, bergantung kepada genus virus tertentu. Walau bagaimanapun, kehadiran protein E telah ditunjukkan untuk mengaktifkan tindak balas keradangan patogen yang boleh menyebabkan kematian dalam model haiwan dan manusia [21, 22].
Protein E sekarang diterima bertanggungjawab untuk sebahagian besar daripada larian keradangan yang disebabkan oleh SARS-CoV [21]. Mengapa sejenis protein kecil seperti protein E boleh meningkatkan secara mendadak replikasi CoV dan meningkatkan patogenik dan virulennya?
Ribut Cytokine & Apoptosis – Sambungan Mitochondria
Satu ciri klinikal biasa pesakit kritikal yang dijangkiti dengan 2019-nCov adalah kepekatan tinggi sitokin dalam plasma mereka. Analisis menunjukkan bahawa 2019-nCoV menyebabkan kluster pneumonia maut dengan persembahan klinikal yang serupa dengan SARS-coV.
Pesakit yang dijangkiti mempunyai kebarangkalian tinggi untuk mengalami sindrom kesusahan pernafasan akut. 75% pesakit menunjukkan radang paru-paru dua hala (menjejaskan kedua-dua paru-paru) [17].
Semasa wabak SARS-CoV dan MERS-CoV, peningkatan jumlah sitokin proinflamasi dalam serum pesakit yang dijangkiti dikaitkan dengan keradangan pulmonari dan kerosakan paru-paru yang luas [24, 25, 38] IL1B, IL6, IL12, IL15, IL17, TNFα. IFNγ, IP10 dan MCP1 adalah antara sitokin yang tinggi yang terdapat dalam pesakit CoV.
Jumlah IL1B, IFNγ, IP10, dan cytokine MCP1 yang tinggi yang mungkin menyebabkan peningkatan sel T-helper-1 (Th1) diaktifkan juga telah dikenal pasti pada pesakit 2019-nCoV [26].
Serupa dengan SARS-CoV, nilai mutlak limfosit pada kebanyakan pesakit pada tahun 2019-nCoV telah dikurangkan dengan nyata, menunjukkan bahawa mekanisme tindakan utama 2019-nCoV dapat diarahkan pada limfosit, terutama limfosit T.
Apabila zarah-zarah virus menyebar dan menjangkiti sel-sel lain, badan bertindak balas dengan tindak balas kekebalan tubuh yang dikenali sebagai ribut sitokin yang menyebabkan perubahan dalam sel darah putih periferal dan sel-sel imun termasuk limfosit. Badai Cytokine mungkin sebabnya mengapa sesetengah pesakit berkembang pesat dengan sindrom kesusahan pernafasan akut dan kejutan septik, diikuti oleh kegagalan organ dan kematian pada akhirnya [17].
2019-nCoV dan The Cytokine Storm
Istilah “Cytokine Storm”, yang pertama kali digunakan pada tahun 1993 [26] menggambarkan fenomena di mana tindak balas keradangan dalam sistem imun keluar dari kawalan [39]. Istilah ini kemudian dikaitkan dengan jangkitan virus termasuk, lymphohistiocytosis hemophagocytic yang berkaitan dengan virus Epstein-Barr, kumpulan A streptokokus, virus influenza, dan SARS-CoV.
Cytokines adalah sekumpulan protein yang dirembeskan oleh sel untuk memberi isyarat dan komunikasi dalam peraturan angiogenesis, tindak balas imun dan keradangan. Protein ini boleh menimbulkan pelbagai tindak balas yang berbeza bergantung kepada sitokin dan sel sasaran.
Keradangan di ribut sitokin biasanya bermula di tapak tempatan dan kemudiannya tersebar ke seluruh tubuh melalui peredaran sistemik.
Gejala seperti kemerahan, bengkak atau edema, haba dan kesakitan adalah ciri-ciri keradangan akut di tapak tempatan. Respons keradangan ini sering terjadi dengan mengorbankan fungsi organ tempatan. Proses pembaikan pampasan biasanya dimulakan selepas keradangan bermula, dan proses pembaikan dalam kebanyakan kes benar-benar boleh memulihkan fungsi tisu dan organ.
Walau bagaimanapun, apabila keradangan yang teruk merosakkan struktur tisu tempatan, penyembuhan hanya boleh meneruskan dengan fibrosis, yang sering menyebabkan disfungsi organ berterusan [28].
SARS-CoV merupakan contoh utama tindak balas ribut sitokin yang mengakibatkan jangkitan paru-paru yang teruk, yang membawa kepada perkembangan fibrosis pulmonari. Manifestasi klinik dari 2019-nCoV nampaknya menyiratkan mekanisme yang serupa, sebagai pesakit yang dijangkiti memamerkan kadar radang paru-paru dua hala yang tinggi [17].
Di kebanyakan cytokine ribosom, protein cytokine-respon akut seperti TNF, IL-1β, IL-8 dan MCP-1 muncul dalam masa beberapa minit selepas berjangkit, diikuti peningkatan IL-6, sementara sitokin IL-10 kelihatan agak kemudian, sebagai badan cuba untuk mengawal respon keradangan akut sistemik, sebagai IL-10 adalah mekanisme pertahanan anti-radang [28]. Dalam jangkitan teruk seperti yang dimulakan oleh C***na virus, tindak balas imun yang normal dimanipulasi oleh virus yang boleh menyebabkan sistem kekebalan tubuh menjadi terganggu.
Apabila badan memulakan pengeluaran sistemik IL-10 apabila ribut sitokin dimulakan, fasa yang dikenali sebagai ‘imunoparalisis’ mengambil alih fungsi neutrophils dan monosit yang dikurangkan dalam usaha untuk mengawal dan memerintah dalam tindak balas keradangan sistemik kepada jangkitan tempatan [29, 30, 31].
Walau bagaimanapun, ada kemungkinan pesakit tidak dapat pulih dari imunoparalisis walaupun mereka selamat dari ribut sitokin awal. Pesakit-pesakit yang mengalami imunosuppression yang teruk akan dicabar dengan permulaan sepsis teruk yang menyebabkan kematian akhirnya [32].
Oleh itu, homeostasis imun adalah kritikal semasa perkembangan ribut sitokin. Ketidakupayaan untuk membersihkan sel apoptosis tepat pada masanya [33] mungkin merupakan salah satu sebab peningkatan virulensi C***na virus semasa ribut sitokin.
Mitokondria, Protein Sampul dan Apoptosis – Kisah Depolarization
Apoptosis adalah fungsi biologi penting yang melibatkan kematian sel untuk tujuan mengawal selia pembiakan sel dan pembezaan dalam tisu sel, serta patogenesis pelbagai penyakit [34]. Laluan biokimia yang diperlukan untuk kematian sel apoptosis adalah di mana-mana SEMUA sel mamalia dan boleh diaktifkan dengan pelbagai isyarat tambahan dan intraselular.
Pada masa ini, diiktiraf secara meluas bahawa mitokondria memainkan peranan penting dalam pengawalan apoptosis [35]. Pada peringkat awal apoptosis, protein pro-apoptosis yang berbeza termasuk cytochrome c biasanya dijumpai di ruang intermembrane dilepaskan ke dalam sitosol. Walau bagaimanapun, langkah utama yang memulakan proses apoptosis ialah PERMEABILISASI membran mitokondria luar [36]. Protokol sampul surat dalam C***na virus mendorong permeabilisasi membran [19, 23].
Protein 3b yang dikodkan oleh SARS-CoV telah dikenalpasti dalam mitokondria. Penyetempatan protein di mitokondria dipercayai menyumbang kepada patogenesis SARS pada manusia [37]. Sementara protein lain yang dikodkan oleh coronavirus SARS-CoV yang dikenali sebagai protein 3a telah ditunjukkan untuk menyebabkan kematian sel yang luas dengan induksi jalur apoptosis mitokondria di mana sitokrom c dilepaskan ke sitosol [41].
Kenapa coronavirus menyebabkan kebolehtelapan membran supaya menyuntik protein menjadi mitokondria, menyebabkan apoptosis dan kematian sel?
Dinamika mitokondria adalah penting dalam kekebalan antivirus
Virus, termasuk C***navirus, mempunyai keupayaan untuk mengubah fungsi selular untuk meningkatkan proliferasi. Keupayaan untuk mengelakkan tindak balas imun adalah mungkin aspek yang paling penting dalam kegigihan dan percambahan virus. Penemuan baru-baru ini telah menunjukkan bahawa mitokondria adalah pengatur pusat sistem imun kita, mengawal isyarat imun semula jadi dan sel-sel sel imun [42].
Membran luar mitokondria telah muncul sebagai platform utama untuk molekul isyarat penting, dan dinamika mitokondria yang melibatkan gabungan dan pembelahan memainkan peranan kritikal dalam pengaktifan sel imun [43]. Imuniti dan mitokondria kini diterima dengan saling berkaitan, kerana mitokondria dapat mengawal pengaktifan, pembezaan dan kelangsungan sel-sel imun [44].
Semasa jangkitan virus, dinamika mitokondria diubah kerana virus memanipulasi dinamarki mitokondria untuk mempengaruhi perkembangan jangkitan. Gangguan dinamika mitokondria yang disebabkan oleh virus, termasuk C***navirus, boleh meningkatkan patogenesis virus [45].
Inilah sebabnya mengapa C***naavirus SARS-CoV yang disandikan protein 3a, 3b mensasarkan mitokondria untuk menimbulkan kerosakan dan kecederaan, menyebabkan apoptosis untuk mensirkulasikan sistem kekebalan tuan rumah [37, 41].
Semasa jangkitan, mitokondria yang rosak biasanya akan dibersihkan dengan cepat melalui proses gabungan dalam dinamarki mitokondria dan mitophagy.
Pembelahan adalah proses yang memudahkan pemisahan mitokondria yang rosak, yang kemudiannya dikeluarkan oleh mitophagy. Mitokondria yang sihat yang sihat akan disatu dengan rangkaian mitokondria sedia ada melalui proses gabungan. Dengan cara ini, mitokondria dapat mengekalkan pengeluaran tenaga untuk mengekalkan homeostasis selular [46].
Walau bagaimanapun, jika mitokondria menjadi sangat depolarized dan oleh itu tidak dapat dipulihkan, mitokondria ini akan dihapuskan secara kekal tanpa kemungkinan reincorporated melalui acara fusion.
Potensi membran mitokondria (ΔΨm) menjadi faktor penentu dalam menyusun mitokondria yang mana dapat diperbaiki dan dipulihkan, dan yang mesti dipisahkan dan disingkirkan secara kekal [45].
Permeabilization Membran dan Depolarization
Permulaan depolarization mitokondria sentiasa ditambah dengan depolarisasi potensi membran plasma. Kajian juga menunjukkan bahawa permeabilisasi membran mitokondria luar adalah perlu bagi depolarisasi potensi membran semasa apoptosis [47]. Permeabilisasi membran mitokondria dan kehilangan potensi transmigran mitokondria, atau depolarisasi ΔΨm sering digunakan sebagai biomarker apoptosis [53]
Semasa depolarisasi mitokondria, pembebasan sejumlah besar cytochrome c melambatkan aliran elektron, mengganggu pengeluaran ATP yang akhirnya membawa kepada pembentukan radikal bebas yang meningkat yang akan mengganggu homeostasis selular [47].
Potensi membran mitokondria (ΔΨm) adalah sumber utama tenaga kimia yang bertanggungjawab untuk memacu semula proton dari ruang intermembrane melalui synthase ATP kembali ke matriks mitokondria [48]. Penyelenggaraan yang sesuai ΔΨm adalah penting untuk pengeluaran tenaga mitokondria kerana tenaga yang tersedia untuk sintesis ATP secara langsung diperolehi daripada potensi membran mitokondria (ΔΨm). Depolarization diterjemahkan ke dalam tenaga yang berkurangan untuk sintesis ATP.
Sekarang difahami bahawa mitokondria mengandungi rumah-rumah kuasa yang saling berkaitan yang dipanggil cristae [49]. Crista individu dapat mengekalkan potensi membran yang berbeza di sepanjang membran mitokondria dalaman. Semasa peristiwa depolarization sementara, sesetengah cristae dapat mengekalkan polariti walaupun keruntuhan ΔΨm di cristae bersebelahan [50].
Ini bermakna semasa depolarization, cristae yang dapat mengekalkan potensi membran boleh diselamatkan dan menyatu menjadi mitochondria yang sihat. Walau bagaimanapun, gabungan mesti berlaku sebelum kristina kehilangan polaritas secara kekal kerana potensi membran berkurang dapat mengurangkan tahap protein fusion OPA1, menghasilkan mitokondria bukan fusing sebagai hasil [51]. Penjejakan secara serentak terhadap pembelahan dan Δψm mendedahkan bahawa mitokondria depolarisasi yang dihasilkan semasa peristiwa pembelahan adalah ENAM kali lebih kecil kemungkinannya disatu dalam masa 10 minit yang akan datang [52].
Apa yang boleh memudahkan penyelamatan mitokondria depolarized?
Asid Ascorbic, Mitokondria & Depolarization – Sistem Redoks Membran Plasma Revisited
Penemuan baru-baru ini menunjukkan bahawa asid askorbik mempunyai keupayaan untuk mengembalikan kadar gabungan mitokondria kepada normal dalam satu model untuk penyakit Parkinson [54]. Banyak kajian terdahulu telah menunjukkan bahawa asid askorbik, vitamin C, boleh mengelakkan kehilangan potensi membran mitokondria.
Apabila sel-sel telah dirawat dengan agen yang tidak dapat menghalang fosforilasi oksidatif seperti CCCP (karbonyl cyanide m-chlorophenyl hydrazone), potensi membran diturunkan bersama induksi permeabilisasi membran, manakala protein sitokrom c dilancarkan untuk memulakan apoptosis. Penambahan asid askorbik ke sel-sel ini menghalang depolarization dan berlaku kejadian lata apoptotik [55].
Keupayaan asid askorbik untuk mencegah depolarisasi dalam membran mitokondria memberikan kesan anti-sitotoksik yang menyebabkan penurunan dos yang bergantung kepada apoptosis dalam sel semasa eksperimen in vitro. [56] Sinaran mengionkan menyebabkan depolarization membran mitokondria dalam sel dan menyebabkan apoptosis [57]. Pretreating sel dengan asid askorbik yang dilindungi sel terhadap sinaran pengionan akibat apoptosis [58].
C***navirus & Depolarization Membran – Sambungan Asid Ascorbic
N-protein SARS-CoV telah ditunjukkan untuk menyebabkan apoptosis melalui laluan apoptosis mitokondria di bawah kelaparan serum. Zhang et al. pada tahun 2009 mendapati bahawa protein N-dapat menyebabkan peningkatan generasi spesies oksigen reaktif, menyebabkan kehilangan potensi membran, kebolehtelapan membran meningkat, pembebasan cytochrome C dan akhirnya kematian sel selepas serum lembu ditarik balik selama 24 jam [59]. Mengapa serum lembu penting? Serum lembu mengandungi pelbagai mikronutrien [60] tetapi kebanyakannya, ia mengandungi asid askorbik [61].
Tidak syak lagi bahawa C***navirus seperti mitokondria sasaran 2019-nCoV, SARS-CoV, dan MERS-CoV untuk mendorong apoptosis untuk mengganggu sistem kekebalan tuan rumah untuk memudahkan percambahan. Melindungi dinamarki mitokondria dalam kejadian fisi dan fisi membolehkan mitokondria depolarized untuk mendapatkan semula kawalan fungsi. Bagaimanakah asid askorbik mengekalkan potensi membran untuk melindungi dinamarki mitokondria?
CYB5R3 & VDAC1 – Kisah Potensi Membran & Asid Ascorbic
Terdapat rangkaian enzim membran plasma yang luas, dinamik dan berpengaruh yang mengawal keseimbangan redoks dalam persekitaran selular. Enzim-enzim ini tidak diklasifikasikan secara rasmi sehingga awal 2000 kerana mereka terutamanya NADH atau NADPH oksida yang dikenali di bawah pelbagai nama lain berdasarkan kepada penerima elektron fisiologi mereka. Kebanyakan enzim membran plasma redoks yang telah dikenal pasti setakat ini menggunakan asid askorbik hampir EKSKLUSIF sebagai penerima elektron dan penderma mereka, kerana ciri-ciri unik asid askorbik [62].
Enzim membran plasma CYB5R dikodkan oleh empat gen CYB5R1, CYB5R2, CYB5R3 dan CYB5R4. CYB5R3 isoform mempunyai ungkapan sitoplasma di mana-mana dan bentuk membrannya wujud dalam mitokondria, nukleus, retikulum endoplasma dan membran plasma [64].
CYB5R3 (membran terikat NADH: cytochrome b5 oxidoreductase 3) enzim mempelbagaikan pertukaran elektron yang cepat antara ascorbate dan satu metabolit pengoksidaan elektron, radikal bebas ascorbyl (AFR), juga dikenali sebagai semidehydroascorbate. Enzim CYB5R3 menggunakan elektron daripada NADH untuk menukar AFR ke dalam ascorbate [64].
CYB5R3 terletak pada membran mitokondria luar dan berfungsi secara fungsional kepada VDAC1 (saluran anion yang bergantung kepada voltan 1). VDAC1 adalah protein yang paling banyak terdapat pada membran mitokondria luar (OMM) [64]. Sistem Cyb5R3 / VDAC1 bertanggungjawab untuk penukaran AFR ke dalam ascorbate. VDAC1 telah ditunjukkan untuk mengekalkan integriti membran mitokondria, menjaga sel-sel utuh apabila terdedah kepada karsinogen yang boleh menyebabkan depolarization dan apoptosis [65, 66].
Tikus dibiakkan tanpa CYB5R3 menunjukkan kehilangan biogenesis mitokondria, disertai dengan kehilangan 30% jumlah ATP, 50% kehilangan aktiviti Kompleks IV, dan kehilangan protein Kompleks IV 25% [67]. Kenapa CYB5R3 penting untuk mengekalkan fungsi normal mitokondria, termasuk aktiviti mitokondria ETC, penggunaan oksigen, pengeluaran ATP dan penentangan terhadap tekanan oksidatif? CYB5R3 / VDAC1 sebenarnya merupakan laluan penjanaan tenaga tambahan yang menggunakan ascorbate / AFR sebagai penderma elektron dan penerima [68].
Apabila aktiviti fosforilasi oksidatif tidak disokong oleh protein rantaian pernafasan kerana potensi membran yang runtuh (depolarization), aktiviti sistem CYB5R3 / VDAC1 dapat menghasilkan potensi membran elektrokimia yang dikatalisis oleh pemindahan elektron [69, 70, 71]. Elektron pemindahan CYB5R3 / VDAC1 dari NADH sitosol ke mitokondria, menggunakan Kompleks IV [69, 72]. Paling mengejutkan, apabila asid askorbik, bukannya NADH dibekalkan kepada mitokondria utuh, induksi bukan enzim yang sama pada jalur pengeluaran tenaga alternatif ini diperhatikan, di mana terdapat pengambilan oksigen, pengurangan sitokrom c dan pengoksidasi ascorbate [69,72].
Pertukaran pesat AFR kembali kepada askorbor menggunakan NADH sebagai penderma elektron mengembalikan kolam askorbat dan mengekalkan nisbah NAD + / NADH tinggi dalam sel [68]. Walau bagaimanapun, jika terdapat kekurangan NADH, maka perlu untuk mengekalkan bekalan tetap ascorbate segar supaya CYB5R3 / VDAC1 dapat menggunakan elektron daripada askorbor untuk menghasilkan potensi membran untuk menyelamatkan depolariisasi mitokondria.
Semasa jangkitan teruk, keupayaan mitokondria untuk menggunakan sistem redoks plasma CYB5R3 / VDAC1 untuk menjana bekalan sementara tenaga alternatif akan memberikan mitokondria peluang untuk mengekalkan kejadian fisi dan pembelahan untuk membersihkan mitokondria yang rosak. Asid askorbik menyediakan elektron kepada CYB5R3 / VDAC1 apabila NADH tidak mencukupi disebabkan oleh fosforilasi oksidatif yang terganggu.
Kepentingan bekalan berterusan asid askorik yang mencukupi semasa ribut sitokin yang disebabkan oleh jangkitan C***navirus tidak boleh dipandang rendah.
Bottom Line
Sekarang dah macam wabak dah kan sebelum ni influenza, sekarang kecoh dengan C***navirus pula, kadang tu tak tau kenapa, tiba-tiba melanda. Jumlah kematian juga semakin bertambah disebabkan virus baru ni 2019-nCoV.
Sebaiknya ambik langkah pencegahan. Pencegahan bukan sahaja dari sudut ambil suplemen, tapi jaga kebersihan dan pemakanan sekali.
Suplemen pun kalau mampu, belikanlah untuk anak-anak. Ini yang saya selalu buat. Saya kerja keras, saya sayang anak-anak, saya belikan suplemen untuk mereka disamping ambil langkah pencegahan yang lain.
Dan kita dah tau pun C***navirus 2019-nCoV ni pun sangat bahaya sehingga boleh sebabkan kematian, lebih baik kita mencegah.
Bagaimana Nak Beli Set C***naVirus?
Sila hubungi 012-2195919 atau klik link di bawah
Klik untuk Beli Set C***naVirus Shaklee
Semoga perkongsian ini bermanfaat untuk semua dan jika anda ingin mendapatkan produk Shaklee atau menyertai Shaklee boleh hubungi saya dan saya akan membantu anda turut sama berjaya.
Raihanah SID 864679
No tel: 0122195919
Your trusted Shaklee Independent Distributor
Beauty Consultant
Shaklee Gombak
References
[1] Novel Coronavirus 2019 Situation Summary, Wuhan, China | CDC https://www.cdc.gov/coronavirus/2019-ncov/summary.html
[2] Ascorbic acid: its role in immune system and chronic inflammation diseases. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/24766384
[3] Mechanisms of attenuation of abdominal sepsis induced acute lung injury by ascorbic acid. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/22523283
[4] Vitamin C and Immune Function https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5707683/
[5] Effects of ascorbate on leucocytes: Part III. In vitro and in vivo stimulation of abnormal neutrophil motility by ascorbate. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/550365
[6] Lymphocytes 2018_Influence of Vitamin C on Lymphocytes: An Overview https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5874527/
[7] Technical advance: ascorbic acid induces development of double-positive T cells from human hematopoietic stem cells in the absence of stromal cells. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/25157026/
[8] Promotion of IL-4- and IL-5-dependent differentiation of anti-mu-primed B cells by ascorbic acid 2-glucoside. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/19201381/
[9] Vitamin C and Infection | Nutrition Reviews | Oxford Academic https://academic.oup.com/nutritionreviews/article-abstract/1/7/202/1874601?redirectedFrom=PDF
[10] Vitamin C and Infections. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/28353648/
[11] Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding – The Lancet https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30251-8/fulltext
[12] Interspecies transmission and emergence of novel viruses: lessons from bats and birds. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/23770275
[13] Middle East respiratory syndrome coronavirus: another zoonotic betacoronavirus causing SARS-like disease. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/25810418
[14] ACE2 receptor expression and severe acute respiratory syndrome coronavirus infection depend on differentiation of human airway epithelia. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/16282461
[15] Single-cell RNA expression profiling of ACE2, the putative receptor of Wuhan 2019-nCov | bioRxiv https://www.biorxiv.org/content/10.1101/2020.01.26.919985v1
[16] Functional assessment of cell entry and receptor usage for lineage B β-coronaviruses, including 2019-nCoV | bioRxiv https://www.biorxiv.org/content/10.1101/2020.01.22.915660v1.full
[17] Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study – The Lancet https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30211-7/fulltext
[18] Functional assessment of cell entry and receptor usage for lineage B β-coronaviruses, including 2019-nCoV | bioRxiv https://www.biorxiv.org/content/10.1101/2020.01.22.915660v1.full#ref-20
[19] Expression of SARS-coronavirus envelope protein in Escherichia coli cells alters membrane permeability. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/15522242/
[20] Biochemical and functional characterization of the membrane association and membrane permeabilizing activity of the severe acute respiratory syndrome coronavirus envelope protein.- PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/16507314/
[21] CORONAVIRUS VIRULENCE GENES WITH MAIN FOCUS ON SARS-CoV ENVELOPE GENE https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4261026/
[22] Coronavirus envelope protein: current knowledge | Virology Journal | Full Text https://virologyj.biomedcentral.com/articles/10.1186/s12985-019-1182-0
[23] Genomic characterization of the 2019 novel human-pathogenic coronavirus isolated from a patient with atypical pneumonia after visiting Wuhan: Emerging Microbes & Infections: Vol 9, No 1 https://www.tandfonline.com/doi/full/10.1080/22221751.2020.1719902
[24] Plasma inflammatory cytokines and chemokines in severe acute respiratory syndrome https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1808997/
[25] MERS-CoV infection in humans is associated with a pro-inflammatory Th1 and Th17 cytokine profile. – PubMed – NCB Ihttps://www.ncbi.nlm.nih.gov/pubmed/29414327
[26] Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China – The Lancet https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)30183-5/fulltext
[27] Cytokine storm of graft-versus-host disease: a critical effector role for interleukin-1. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/8442093
[28] Into the Eye of the Cytokine Storm https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3294426/
[29] Development of the adult respiratory distress syndrome: progressive alteration of neutrophil chemotactic and secretory processes. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1900478/
[30] Monocyte deactivation in septic patients: restoration by IFN-gamma treatment. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/9176497
[31] Normal responses to injury prevent systemic inflammation and can be immunosuppressive. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/11179099
[32] Persisting low monocyte human leukocyte antigen-DR expression predicts mortality in septic shock. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/16741700
[33] Apoptotic Cells Induced Signaling for Immune Homeostasis in Macrophages and Dendritic Cells https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5661053/
[34] Apoptosis: A Basic Biological Phenomenon with Wideranging Implications in Tissue Kinetics | British Journal of Cancer https://www.nature.com/articles/bjc197233
[35] Mitochondrial regulation of apoptotic cell death – ScienceDirect https://www.sciencedirect.com/science/article/abs/pii/S037842740300479X
[36] Multiple pathways of cytochrome c release from mitochondria in apoptosis – ScienceDirect https://www.sciencedirect.com/science/article/pii/S0005272806000715
[37] Mitochondrial location of severe acute respiratory syndrome coronavirus 3b protein. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/16682811
[38] Active Replication of Middle East Respiratory Syndrome Coronavirus and Aberrant Induction of Inflammatory Cytokines and Chemokines in Human Macrophages: Implications for Pathogenesis | The Journal of Infectious Diseases | Oxford Academic ttps://academic.oup.com/jid/article/209/9/1331/884110
[39] Mapping the innate signaling cascade essential for cytokine storm during influenza virus infection | PNAS https://www.pnas.org/content/111/10/3799
[40] Host cell proteases: critical determinants of coronavirus tropism and pathogenesis https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4465284/
[41] Severe acute respiratory syndrome coronavirus 3a protein activates the mitochondrial death pathway through p38 MAP kinase activation https://www.ncbi.nlm.nih.gov/pubmed/18632968
[42] Mitochondria as central hub of the immune system – ScienceDirect https://www.sciencedirect.com/science/article/pii/S2213231719303076
[43] Mitochondria are the powerhouses of immunity | Nature Immunology https://www.nature.com/articles/ni.3704?draft=marketing
[44] Diverse Roles of Mitochondria in Immune Responses: Novel Insights Into Immuno-Metabolism | Immunology https://www.frontiersin.org/articles/10.3389/fimmu.2018.01605/full
[45] Mitochondrial dynamics and viral infections: A close nexus – ScienceDirect https://www.sciencedirect.com/science/article/pii/S0167488915000099
[46] The essential role of mitochondrial dynamics in antiviral immunity https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5988924/
[47] Outer mitochondrial membrane permeabilization during apoptosis triggers caspase-independent mitochondrial and caspase-dependent plasma membrane potential depolarization: a single-cell analysis | Journal of Cell Science https://jcs.biologists.org/content/116/3/525
[48] Coupling of Phosphorylation to Electron and Hydrogen Transfer by a Chemi-Osmotic type of Mechanism | Nature https://www.nature.com/articles/191144a0
[49] Cristae – The Powerhouses Within – EvolutaMente.it https://www.evolutamente.it/cristae-the-powerhouses-within/
[50] Individual cristae within the same mitochondrion display different membrane potentials and are functionally independent | The EMBO Journal https://www.embopress.org/doi/full/10.15252/embj.2018101056
[51] Fission and selective fusion govern mitochondrial segregation and elimination by autophagy https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2234339/
[52] Fission and selective fusion govern mitochondrial segregation and elimination by autophagy. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/18200046/
[53] Role of mitochondrial membrane permeabilization and depolarization in platelet apoptosis – Leytin – 2018 – British Journal of Haematology – Wiley Online Library https://onlinelibrary.wiley.com/doi/full/10.1111/bjh.14903
[54] Exploring the Effect of Rotenone—A Known Inducer of Parkinson’s Disease—On Mitochondrial Dynamics in Dictyostelium discoideum https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6262481/
[55] Vitamin C enters mitochondria via facilitative glucose transporter 1 (Glut1) and confers mitochondrial protection against oxidative injury | The FASEB Journal https://www.fasebj.org/doi/full/10.1096/fj.05-4107com?ck=nck&legid=fasebj%3B19%2F12%2F1657&cited-by=yes
[56] Vitamin C Antagonizes the Cytotoxic Effects of Antineoplastic Drugs | Cancer Research https://cancerres.aacrjournals.org/content/68/19/8031
[57] Ionizing radiation-induced, mitochondria-dependent generation of reactive oxygen/nitrogen. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/11358802
[58] Ascorbic acid inhibits apoptosis induced by X irradiation in HL60 myeloid leukemia cells. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/10521923?dopt=Abstract
[59] SARS-CoV Nucleocapsid Protein Induced Apoptosis of COS-1 Mediated by the Mitochondrial Pathway: Artificial Cells, Blood Substitutes, and Biotechnology: Vol 35, No 2 https://www.tandfonline.com/doi/full/10.1080/10731190601188422#
[60] The Influence of Micronutrients in Cell Culture: A Reflection on Viability and Genomic Stability https://www.hindawi.com/journals/bmri/2013/597282/
[61] Chiral analysis of ascorbic acid in bovine serum using ultrathin molecular imprinted polyaniline/graphite electrode – ScienceDirect https://www.sciencedirect.com/science/article/pii/S1572665717302953
[62] Thioredoxin Reductase AFR NADH NADPH_Molecular biology of mammalian AFR reductases https://www.researchgate.net/publication/236015879_Molecular_biology_of_mammalian_AFR_reductases
[63] Characterization of the Trans-plasma Membrane Electron Transport System in the Myelin Membrane https://scholars.wlu.ca/cgi/viewcontent.cgi?referer=https://www.google.com/&httpsredir=1&article=2785&context=etd
[64] External mitochondrial NADH-dependent reductase of redox cyclers: VDAC1 or Cyb5R3? – ScienceDirect https://www.sciencedirect.com/science/article/abs/pii/S0891584914002573?via%3Dihub
[65] Paraquat toxicity induced by voltage-dependent anion channel 1 acts as an NADH-dependent oxidoreductase. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/19717555
[66] Paraquat induces oxidative stress and neuronal cell death; neuroprotection by water-soluble Coenzyme Q10. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/15519605
[67]Cytochrome B5 Reductase 3 Is Essential for Cardiomyocyte Function | Circulation https://www.ahajournals.org/doi/abs/10.1161/circ.136.suppl_1.20733
[68] Vitamin C versus Cancer: Ascorbic Acid Radical and Impairment of Mitochondrial Respiration? https://new.hindawi.com/journals/omcl/2020/1504048/
[69] Modulation of Cytochrome c-Mediated Extramitochondrial NADH Oxidation by Contact Site Density – ScienceDirect https://www.sciencedirect.com/science/article/abs/pii/S0006291X99907878
[70] Membrane potential generation coupled to oxidation of external NADH in liver mitochondria. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/9762923
[71] Cytochrome c-induced cytosolic nicotinamide adenine dinucleotide oxidation, mitochondrial permeability transition, and apoptosis. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/12573279
[72] Porin and cytochrome oxidase containing contact sites involved in the oxidation of cytosolic NADH. – PubMed – NCBI https://www.ncbi.nlm.nih.gov/pubmed/15752713



semoga Allah melindungi kita semua dan memberikan kesihatan kepada kita..kita sebagai manusia perlu berusaha untuk mencegah penyakit2 nih…
Berat nya post ni. Hahahha menari2 sel tu semua bila baca.
Rawlins memang mengamalkan Vit C sekarang. Ditambah dengan makan pelbagai buahan. Pastu kurangkan pergi tempat sesak untuk elakkan bertemu ramai orang.
Rawlins GLAM recently posted…Swag, Blossom and Mismis: Local Products Aiming for the World Market
Buat masa sekarang Sis hanya minum Falavettes atau Kordels tu je setiap pagi..VitC le tu..tak pernah amik supllemen memana lagi…lagipun ada sakit ni, kena rujuk Dr baru berani makan ubat lain..
Ni harap esok nak ke airport takde la sebarang konflik berlaku..takut gak ni..
Sis Lin recently posted…KEREPEK NGAKU SEDAP DIMAKAN TAPI NAK MEMBUATNYA PENUH KESABARAN
Wah penulisan yang cukup informatif dan lengkap macam doktor. Good sharing.
what an informative article. I get so much information about this here.
menarik dapat baca info lengkap pasal virus yang menyerang kita sekarang. bagus Shaklee sebab menghasilkan produk vitamin c yang boleh membantu imunisasi badan
menarik dapat baca info lengkap pasal virus yang menyerang kita sekarang. bagus Shaklee sebab menghasilkan produk vitamin c yang boleh membantu imunisasi badan diwaktu genting sekarang
xulhlmi recently posted…MASA UNTUK UBAH HIDUP BERSAMA DR AZIZAN OSMAN – #NUH2020
hari tu ada terbaca tentang shaklee corona ni. ramai yg bash. entahlah. apa2pun terima kasih share artikel yang penuh dengan fakta2. ada yang saya baca sampaikan tak berapa faham sebab istilah saintifik nya 🙂
Wow panjang lebar penerangan di atas ? Saya pun selama ni takfaha sangat pasal virus ni, thanks for sharing!
Princesa3290 recently posted…Erase by MKhan : Instant . Whitening . Flawless .
wah lengkap macam tesis dah. Tapi penting supaya info dapat disampaikan. Jadi set ini adalah sebagai immune booster dan pencegahan kan? Yg sy faham jika imun kita kuat, insyaallah sistem kita dapat tangkis virus ni.
Owhhh cepat ya Shaklee buat kajian utk menapis corona virus. Baca jugak sebelum nie mengenai hal shaklee corona nie, ramai juga yg hentam. Apa2 pon, kita ikhtiar.
Bila baca bab2 virus yang menyerang dunia sekarang memang rasa ngeri sangat. Apa pun moga kita dilindungi
Sis sekarang ni pun risau je nak keluar ke tempat yang ramai orang, dah macam2 virus pulak ada. Sis dah pernah kena Influenza A..seksa rasanya..harap kita semua dijauhkan dari sebarang penyakit yang merbahaya